Vous êtes ici : Accueil Cité des Énergies > ACCUEIL BIAM > Recherche > EBMP > Thèmes de recherche et projets EBMP
Thèmes de recherche
1. De la perception à l'homéostasie des nutriments et à la croissance de biomasse
La croissance photosynthétique repose sur un apport équilibré d’énergie solaire, de CO2 et de nutriments (azote, phosphate, fer…). Face à un environnement fluctuant (disponibilité des nutriments, augmentation de la température, pénurie d’eau, fluctuation des niveaux de CO2…), les cellules doivent constamment ajuster leur métabolisme pour assurer leur survie. Afin d’augmenter la productivité de la biomasse et de rendre les plantes plus résilientes à un environnement changeant, il est nécessaire de comprendre les mécanismes qui sous-tendent la récupération/la détection/l’homéostasie des nutriments et leur importance dans la capture/l’utilisation du CO2. Nos principaux objectifs sont de disséquer l’interaction entre les voies métaboliques du carbone, du fer, de l’azote et du phosphate chez les plantes et les algues (par exemple, à travers l’étude de la photorespiration et de l’exploration du sol par les racines). Pour comprendre les réponses au phosphate et au fer et leur impact sur l’homéostasie des lipides et le stockage du triacylglycérol (TAG), nous tirerons particulièrement profit des outils de pointe de biologie cellulaire permettant de disséquer in vivo la signalisation et l’homéostasie de ces nutriments
2. De la capture photosynthétique du CO2 au stockage du carbone
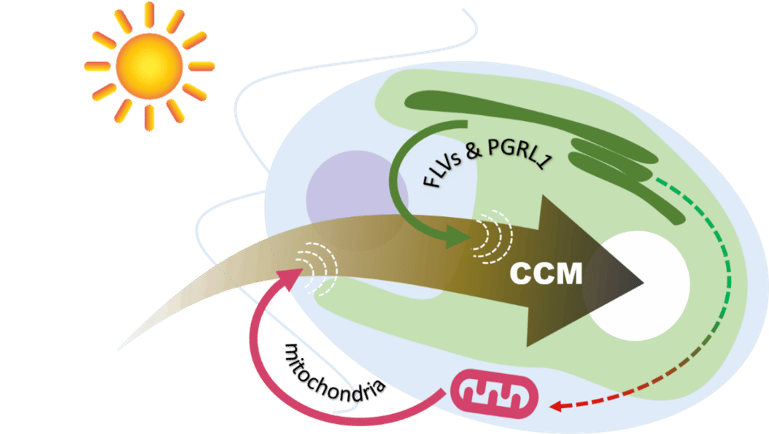
Contenir l’augmentation de la concentration en CO2 atmosphérique et limiter le réchauffement climatique constituent des défis majeurs pour notre société. Grâce à la photosynthèse, plantes et algues sont capables de fixer efficacement le CO2 et sont à la source d’une bioéconomie durable. Domestiquer la photosynthèse pour la production de biomasse ou de composés de réserves comme les lipides ou les sucres représente un enjeu considérable. Au cours de la photosynthèse, l’énergie solaire est captée pour les antennes chlorophylliennes, puis transformée en énergie chimique par diverses voies de transfert d’électrons, l’énergie ainsi transformée servant à alimenter les réactions métaboliques de fixation du CO2. Dans la nature, les végétaux sont soumis à des variation constantes de leur environnement (intensité lumineuse, disponibilité en nutriments, température, …) ce qui affecte les processus biologiques de capture, de transformation et d’utilisation de l’énergie de manière différentielle, et nécessite des régulations extrêmement efficaces afin d’éviter des effets délétères. Nos recherches visent à identifier les mécanismes régulateurs impliqués au niveau des réactions de transfert d’électrons (études des flux d’électrons dissipateurs de type alternatifs) ou de la réorientation du métabolisme vers des voies de stockage du carbone et de l’énergie (TAG ou glycanes), l’objectif final étant de mieux comprendre comment ces voies interagissent dans un environnement fluctuant pour favoriser la capture, la fixation et le stockage du CO2.
3. Mécanismes de synthèse et d’accumulation des lipides de réserve
Les microalgues ont une forte capacité à synthétiser les acides gras et à les accumuler sous forme de réserves en huile (jusqu’à 50 % de leur poids sec). Les acides gras (ou dérivés) extraits de la biomasse algale ont des applications potentielles importantes dans les biocarburants (biodiesel, biopétrole), la nutrition humaine (acides gras polyinsaturés dits oméga 3) et la chimie verte (synthons pour des biopolymères, lubrifiants, etc.). Cependant, des verrous biologiques majeurs restent à lever pour assurer la rentabilité de la filière. Ainsi, l’accumulation d’huile dans les microalgues n’intervient qu’en conditions de stress, notamment une carence nutritive, ce qui limite la croissance cellulaire et donc les productivités en biomasse et en huile. De plus, les applications biocarburants et nutrition humaine requièrent une amélioration de la « qualité » de l’huile de microalgue, c’est-à-dire une optimisation de la composition en acides gras, adaptée à chaque cas.
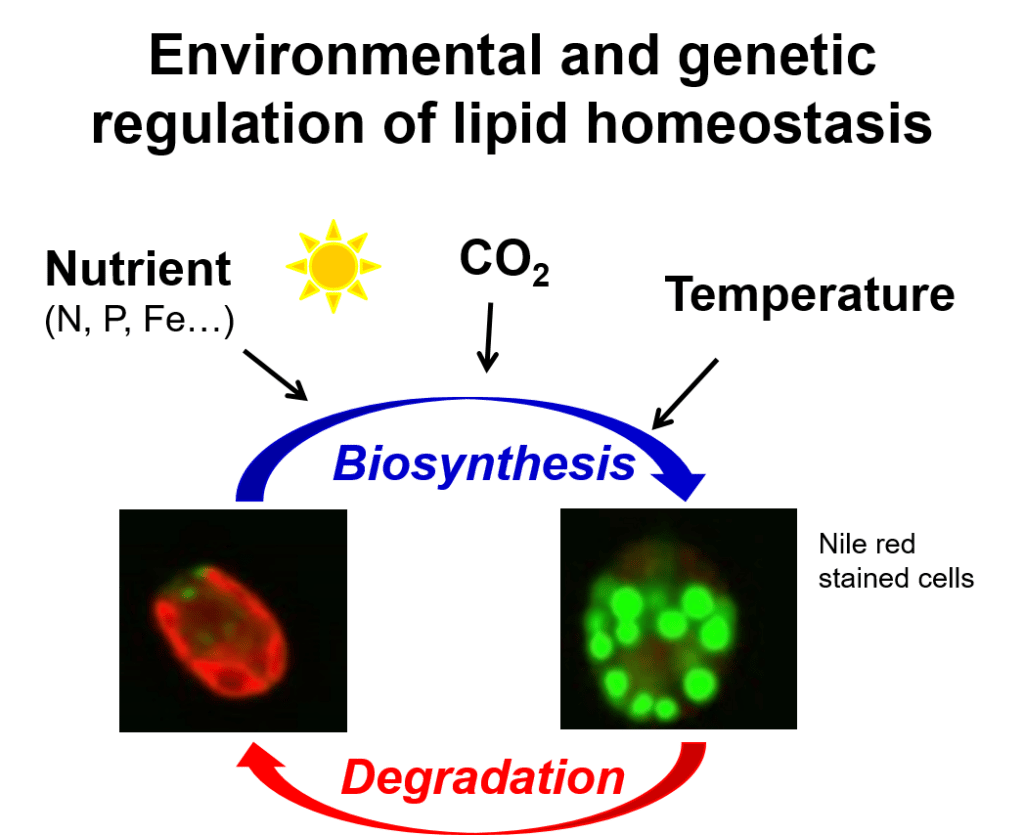
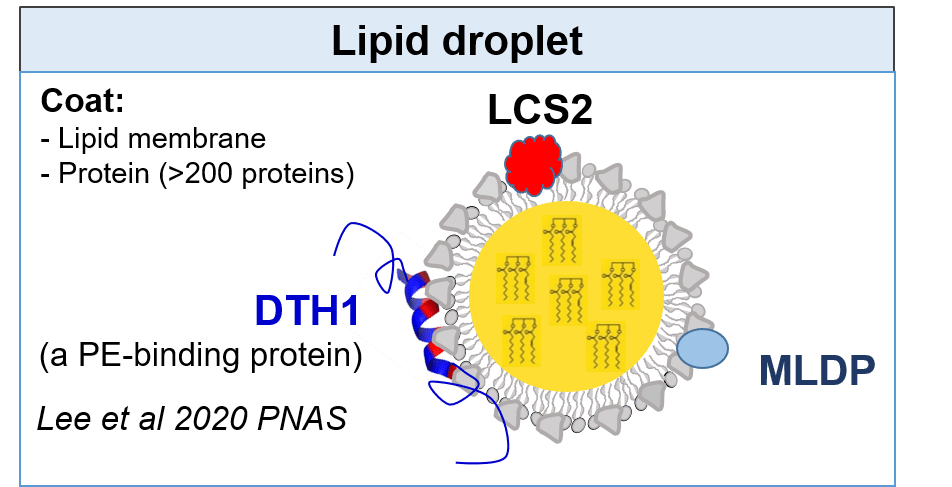
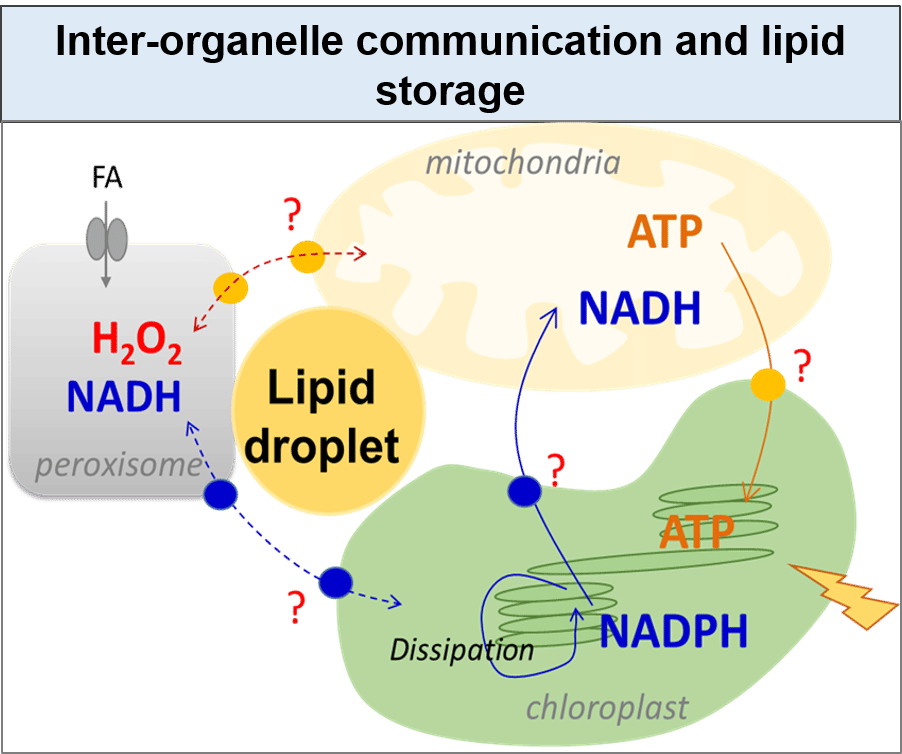
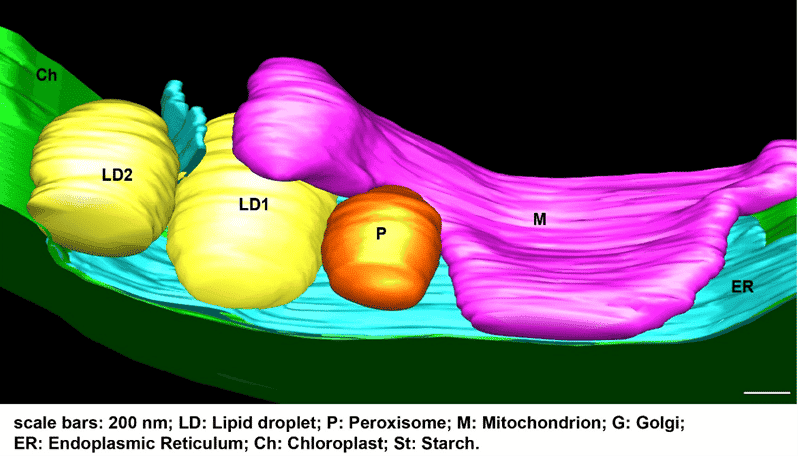
Les recherches menées ont pour but de comprendre les voies de synthèse des lipides de réserve (triacylglycérols) et leurs régulations en relation avec les conditions environnementales (lumière, carence en azote, etc.) et le métabolisme énergétique (photosynthèse). Elles sont menées principalement chez la microalgue modèle Chlamydomonas reinhardtii. Les travaux sont basés sur une approche de génétique formelle visant à isoler des mutants affectés dans leurs capacités à accumuler ou à déstocker l’huile dans diverses conditions de culture (notamment en condition de croissance optimale), ainsi que des mutants dont le profil d’acides gras est modifié. Le criblage des mutants est réalisé par des méthodes haut-débit (cytomètre en flux, GC-MS avec préparation automatisée des échantillons). Après identification de gènes d’intérêt et caractérisation fine des mutants isolés par analyse lipidomique (LC-MS/MS), des stratégies innovantes d’amélioration de la teneur en huile et de sa qualité sont proposées.


4. Biosynthèse et fonction des biohydrocarbures (alcanes, alcènes)
A l’instar de nombreux organismes, les microalgues et les cyanobactéries sont capables de synthétiser alcanes/alcènes linéaires à partir des acides gras constituant leurs lipides (membranaires ou de réserve). La fonction biologique des biohydrocarbures de microorganismes est encore assez énigmatique. Alcanes et alcènes se trouvent aussi être des composants des carburants fossiles et pour la chimie fine. Dans une optique de production de biocarburants lipidiques dans des microorganismes, les alcanes/alcènes ont sur les acides gras et dérivés (huile) l’avantage d’être volatiles. L’excrétion d’alcanes et d’alcènes par des microorganismes et leur capture en phase gaz des cultures, permettrait non seulement de s’affranchir des étapes les plus coûteuses (récolte de la biomasse, traitement par liquéfaction hydrothermale ou extraction de l’huile et conversion en biodiesel), mais aussi d’obtenir des carburants prêts à l’emploi plus purs et donc moins polluants que les carburants fossiles actuels.
Les recherches menées au laboratoire sur les biohydrocarbures ont pour but :
i) D’élucider la fonction biologique des hydrocarbures produits naturellement par les microalgues et les cyanobactéries
ii) D’identifier les enzymes permettant la biosynthèse des hydrocarbures
iii) D’étudier les propriétés, le mécanisme et les relation structures-fonction de ces enzymes
iv) D’exploiter ces connaissances pour explorer les applications visant à produire des hydrocarbures biosourcés.
Nos travaux ont notamment permis d’identifier l’enzyme responsable de la synthèse des alcanes/alcènes chez les microalgues, la fatty acid photodecarboxylase (FAP, voir schéma ci-dessous). C’est une photoenzyme, un type d’enzyme rare qui a besoin d’absorber un photon à chaque cycle catalytique.
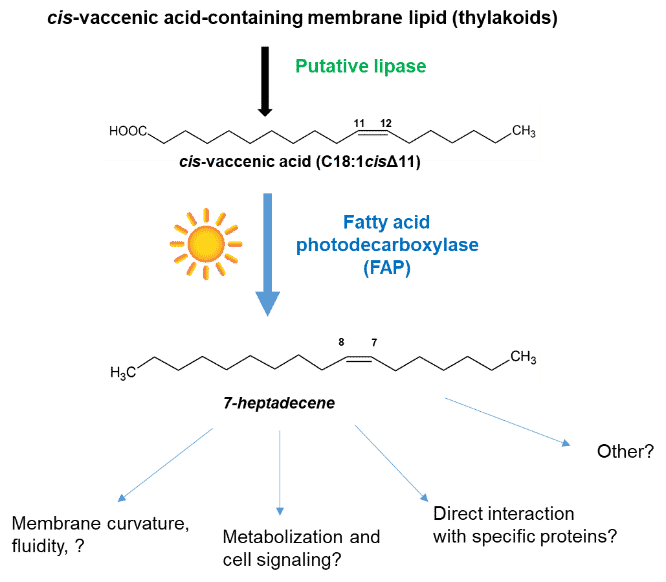
Nos recherches sur la conversion enzymatique d’acides gras s’étendent aussi à la fonctionnalisation des acides gras. Ces travaux, aussi menés en vue d’applications en chimie verte, visent à identifier chez les microalgues ou les plantes de nouvelles enzymes permettant l’introduction de groupements fonctionnels (hydroxy, époxy, etc.) à des positions particulières de la chaîne carbonée des acides gras.
Mots clés
Lipid; Lipidomics; Fatty acids; Lipid droplet; Hydrocarbons
alkanes; Bio-hydrogen; Photosynthesis; Photoenzyme
Energy trafficking; Carbon metabolism; Genetic engineering; Synthetic biology; Chlamydomonas reinhardtii; Nannochloropsis sp